7. November 2014
Dem Neokortex bei der Entwicklung zusehen
IST Austria Professor präsentiert neue Erkenntnisse zur Gehirnentwicklung in der aktuellen Ausgabe von Cell • Hippenmeyer und Ko-AutorInnen verwenden Mosaic Analysis with Double Markers (MADM) um zu dekodieren, wie neokortikale Neuronen entstehen • MADM Methode erlaubt einen quantitativen Blick auf die Zellteilung von einzelnen Stammzellprogenitoren mit einer bisher nicht gekannten Auflösung
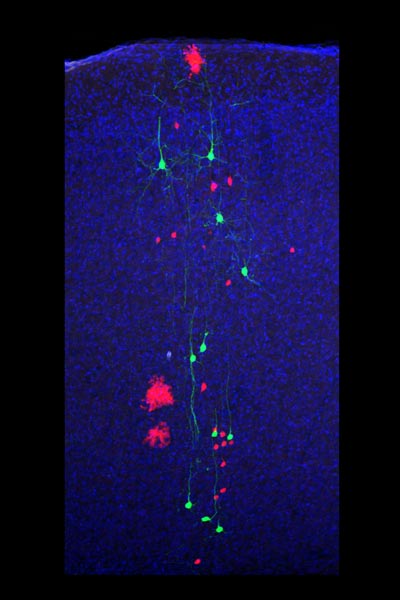
Der Neokortex ist der größte Teil des menschlichen Gehirns und kontrolliert alle höheren kognitiven Funktionen wie das bewusste Denken, die Kontrolle der Bewegung, und die Sinneswahrnehmung. In einer Publikation, die am 6. November in Cell erscheint, präsentiert Simon Hippenmeyer, Assistant Professor am Institute of Science and Technology Austria (IST Austria), mit beispielloser Auflösung wie Neuronen und Gliazellen im Neokortex entstehen. Für diese Forschung arbeitete Simon Hippenmeyer‘s Forschungsgruppe eng zusammen mit Ekaterina Papoucheva von der Bioimaging Facility des IST Austria, dem Labor von Songhai Shi am Sloan Kettering Institute (NY, USA) und Liqun Luo an der Stanford University (CA, USA), sowie mit dem Physiker Benjamin Simons an der Cambridge University (UK) und dem Computerwissenschaftler Kun Huang an der Ohio State University (USA).
Der Neokortex baut sich von innen nach außen auf. Neuronen entstehen, wenn sich radiale Gliavorläuferzellen (englische Abkürzung: RGPs) teilen. Frühgeborene Neuronen bleiben nahe an der Schicht der RGPs, während später geborene Neuronen an den frühgeborenen Neuronen vorbei wandern und Schichten näher an der Oberfläche bilden. Früh- und spätgeborene Neuronen unterscheiden sich auch in ihrer Funktion: Während frühgeborene Neuronen hauptsächlich Verbindungen mit anderen Gehirnarealen außerhalb des Neokortex bilden, verknüpfen sich die spätgeborenen Neuronen bevorzugterweise mit anderen Neuronen innerhalb des Neokortex auf derselben oder der gegenüberliegenden Gehirnhälfte. Bis jetzt war unklar, wie sich RGPs teilen, um die verschiedenen kortikalen Neuronen zu produzieren. Simon Hippenmeyer und Ko-AutorInnen verwendeten nun die Mosaic Analysis with Double Markers (MADM) Technik, um die Prinzipien der Entstehung von exzitatorischen Neuronen im Neokortex von Nagern auf der Einzelzellebene zu entschlüsseln.
Die MADM Technik ist ein beispielloser Ansatz, weil sie es den ForscherInnen erlaubt, die Zellteilungsmuster der Stammzellenvorläufer quantitativ zu betrachten, und die präzise Zelllinie einzelner RGPs zu verfolgen. Die AutorInnen zeigen, dass RGPs einem auffallend deterministischen und koordinierten Entwicklungsprogramm folgen. Alle RGPs teilen sich zunächst symmetrisch und produzieren so einen größeren Pool an Vorläuferzellen. Nach einiger Zeit hört diese symmetrische Teilung auf. Die RGPs teilen sich nun asymmetrisch und produzieren Neuronen. Interessanterweise produzieren RGPs, wenn sie in die neurogene Phase eintreten, jeweils eine definierte Einheit von rund acht Neuronen, was auf einen einheitlichen Output der RGPs hinweist. Die vorausgehenden symmetrischen Teilungen der RGPs scheinen die Anzahl dieser Einheiten zu vergrößern. Exzitatorische Neuronen im Neokortex werden daher vermutlich in „Quanten“ produziert.
Alle RGPs erzeugen neuronale Einheiten, die verschiedene Arten von Neuronen beinhalten – früher-geborene, tiefschichtige Neuronen und später-geborene, oberflächliche Neuronen. Simon Hippenmeyer und KollegInnen bringen so klare Belege für ein Modell, demzufolge RGPs multipotent sind und so zu den Pools der meisten, wenn nicht aller, Hauptarten von kortikalen Projektionsneuronen beitragen.
Die ForscherInnen untersuchten auch was passiert, wenn sie den Transkriptionsfaktor OTX1 entfernen. Dieser bindet DNA und reguliert, welche Gene ein- und welche ausgeschalten sind. OTX1 ist in RGPs in den frühen Stadien der Neuronenproduktion exprimiert und aktiv. Daher wurde bisher angenommen, dass OTX1 nur eine Rolle in der Produktion von früh-geborenen Neuronen spielt. Simon Hippenmeyer und KollegInnen zeigen nun, dass das Entfernen von OTX1 zu einer Reduktion von sowohl früh- als auch spätgeborenen Neuronen führt. Generell gesehen könnten diese Ergebnisse Konsequenzen für unser Verständnis von neurologischen Entwicklungsstörungen haben, weil Mutationen in OTX1 schwere Mikrozephalie und Epilepsie verursachen und in Zusammenhang mit Autismus gebracht wurden.
Zuletzt zeigen die Autoren, dass manche RGPs zu einem vorhersagbaren Anteil nach Ende der Neurogenese zur Produktion von Gliazellen übergehen. Diese deterministische Form der Neuronen- und Gliaproduktion könnte eine wichtige Rolle dabei spielen, das richtige Verhältnis von Neuronen zu Gliazellen sicherzustellen. Sie könnte daher für den gesamten Aufbau und die Funktion des Neokortex entscheidend sein. In zukünftigen Studien wird es interessant sein, das Verhalten von Stammzellen und die Einheitsgröße von RGPs in verschiedenen Spezies quantitativ zu begutachten und ihren Zusammenhang zur neokortikalen Expansion im Lauf der Evolution zu bestimmen.



