4. April 2019
Leukozyten vermessen Poren mit Zellkern, um Weg des geringsten Widerstands zu finden
Mobile Zellen wählen größte Porenöffnung und umschiffen so Hindernisse in dichtem Gewebe
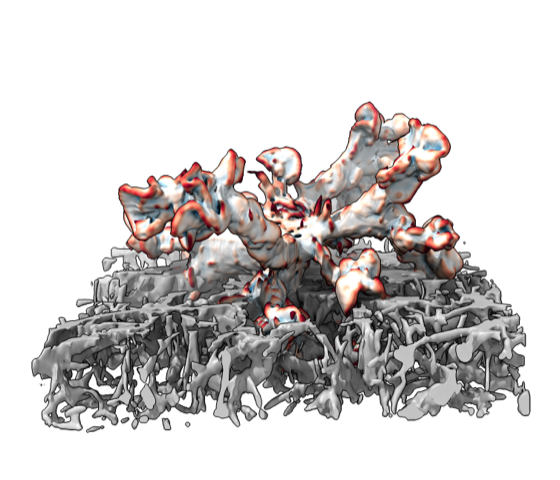
Ein Leukozyt eingebettet in ein 3D-Kollagennetzwerk, visualisiert mittels Lichtblattmikroskopie. © Meghan K. Driscoll, University of Texas Southwestern Medical Center, Dallas, USA
Wie gelangen mobile Zellen wie Leukozyten oder Krebszellen während der Immunüberwachung beziehungsweise der Metastasenbildung an ihren Einsatzort? Die Forschungsgruppe rund um Michael Sixt am Institute of Science and Technology Austria (IST Austria) konnte nun zeigen, dass Leukozyten mithilfe ihres Zellkerns benachbarte Poren vermessen – und so den Weg des geringsten Widerstands finden.
Viele Zellen unseres Körpers müssen mobil sein, um zu ihrem Einsatzort zu gelangen. So legen zum Beispiel im menschlichen Körper alle Leukozyten – die weißen Blutkörperchen des Immunsystems –gemeinsam über 100.000 km pro Stunde zurück. Auf ihrer Reise müssen sich diese Wanderzellen ihren Weg durch ein dreidimensionales Labyrinth bahnen, in dem sich viele weitere Zellen und Elemente der extrazellulären Matrix tummeln. Bestimmte Arten mobiler Zellen, z. B. die Fibroblasten im embryonalen Bindegewebe, fressen sich buchstäblich vorwärts, indem sie das vor sich liegende Gewebe verdauen und somit eine Schneise der Verwüstung zurücklassen. Leukozyten hingegen sind aufgrund ihrer amöboiden Fortbewegungsart nicht nur rund 100 Mal schneller, sondern richten auch keinerlei Schaden in ihrer Umgebung an (würden sich die Leukozyten wie die Fibroblasten im Weg stehendes Gewebe einverleiben, würden sie innerhalb eines Tages Schneisen mit einer Gesamtlänge von über zwei Millionen Kilometern durch den Körper ziehen!). Wie diese extrem schnellen Zellen durch das dichte Gewebenetz navigieren, ohne andere Zellen zu beeinträchtigen, beschäftigt ZellbiologInnen schon lange. Professor Michael Sixt und sein Team – darunter Erstautor Jörg Renkawitz, zur Zeit der Studie Postdoc am IST Austria und nun Leiter einer eigenen Forschungsgruppe am Biomedizinischen Centrum der Ludwig-Maximilians-Universität München –konnten nun beschreiben, wie Leukozyten in komplexen Milieus den Weg des geringsten Widerstands finden.
Zellkern misst Porenweite und navigiert Leukozyten volle Kraft voraus
Um den Mechanismus zu verstehen, der dieser selektiven Art der Zellfortbewegung zugrunde liegt, errichteten die WissenschafterInnen einen Hindernisparcours für Leukozyten in künstlichem Gewebe. Darin folgten die Zellen globalen richtungsweisenden Reizen wie einem chemotaktischen Gradienten und stießen auf ihrem Weg auf Hindernisse unterschiedlicher Porenweite. Wann immer sie die Wahl hatten, entschieden sich die Zellen für die Pore mit dem größten Durchmesser. Durch weitere Tests entdeckten Renkawitz et al., dass diese aktiven zielgerichteten Bewegungen damit zusammenhingen, dass die Zellen ihren Zellkern weit in den vorderen Teil der Zelle verlagert hatten, wo er ihnen als eine Art Maßstab oder Abstandsmesser dient. Anders gesagt, während sich die Zelle vorwärtsbewegt, schiebt sich der in Bewegungsrichtung orientierte Zellkern mithilfe des Zytoskeletts ein Stück weit in mehrere nebeneinander liegende Poren und misst deren Durchmesser. Michael Sixt: „Üblicherweise ist die aktin-reiche Region an der Stirnseite der Zelle verantwortlich für die Erkundung der Umgebung bzw. die Navigation. Was uns überrascht hat, war, dass es bei den Leukozyten anders läuft, denn bei ihnen bestimmt der Zellkern, wo es langgeht – und das macht auch Sinn, da der Zellkern der klobigste Teil der Zelle und gleichzeitig hochempfindlich ist.“
Zugehöriges Video auf YouTube ansehen
Mikrotubuli verhindern Zerstückelung der Zelle beim Porendurchgang
Sobald eine Zelle ihren Zellkern erfolgreich durch eine Pore geschoben hat, muss sie die bereits in benachbarte Poren vorgedrungenen Vorstülpungen ohne Zellkern-Beteiligung wieder zurückziehen, um sich nicht zu verfangen oder gar zerstückelt zu werden. Das Signal zum Rückzug kommt von den Mikrotubuli, die diese Vorstülpungen verlassen, sobald das Mikrotubuli-Organisationszentrum (das direkt an den Zellkern angrenzt), die ausgewählte Pore passiert. Dieses Verschwinden der Mikrotubuli wiederum löst Aktomyosin-Kontraktionen aus, die für den Rückzug der verbliebenen Vorstülpungen sorgen, damit diese dem Zellkern durch die ausgewählte Pore folgen können. Zerstörten die WissenschafterInnen im Experiment die Mikrotubuli, verfingen sich die Zellen in den Poren, da die Vorstülpungen sich nicht zurückzogen, sondern sich weiter durch die von ihnen angesteuerten Poren und somit in verschiedene Richtungen bewegten. Dies führte schlussendlich zur Zerstückelung und zum Tod der Zelle. „Unsere Erkenntnisse basieren auf der Analyse von Leukozyten. Es ist jedoch ziemlich wahrscheinlich, dass sich andere amöboide, bei der Entwicklung, der Immunabwehr oder bei Heilungsprozessen beteiligte Zelltypen genauso verhalten. Darüber hinaus könnte der Mechanismus uns auch helfen, zu verstehen, wie Krebszellen bei der Metastasenbildung von einem Körperteil in einen anderen wandern – und, noch viel wichtiger, wie man sie davon abhalten könnte“, so Michael Sixt abschließend.
Die Studie wurde teilweise durch Daten von KollegInnen der University of Texas Southwestern Medical Center, Dallas, USA, gestützt. Michael Sixts Forschungsarbeit wurde aus Mitteln des European Research Council (ERC), dem Wissenschaftsfonds (FWF) sowie aus Mitteln des FWF DK „Nanocell“ finanziert. Jörg Renkawitz‘ Forschungsarbeit wurde von einer ISTFELLOW-Förderung des People Programme (Marie Curie Actions) des 7. Rahmenprogramms der Europäischen Union (FP7/2007-2013) und einem EMBO Long-Term Fellowship, kofinanziert von der Europäischen Union, getragen.
Publikation:
Jörg Renkawitz, Aglaja Kopf, Julia Stopp, Ingrid de Vries, Meghan K. Driscoll, Jack Merrin, Robert Hauschild, Eric S. Welf, Gaudenz Danuser, Reto Fiolka, & Michael Sixt. 2019. Nuclear positioning facilitates amoeboid migration along the path of least resistance. Nature, DOI: http://dx.doi.org/10.1038/s41586-019-1087-5
Forschungsförderung:
Die Forschungsarbeit am IST Austria im Zuge dieser Studie wurde vom European Research Council (ERC StG 281556 und CoG 724373), einer Förderung des FWF, der FWF-Förderung DK ‘Nanocell’, der ISTFELLOW-Förderung des People Programme (Marie Curie Actions) des 7. Rahmenprogramms der Europäischen Union (FP7/2007-2013; REA-Vertrag Nr. 291734) sowie einem EMBO Long-term Fellowship (ALTF 1396-2014), kofinanziert von der Europäischen Kommission (LTFCOFUND2013, GA-2013-609409), ermöglicht.



