13. Mai 2020
“Off-road”-Modus gibt mobilen Zellen Bewegungsfreiheit
Biomechanisches Grundprinzip der Zellmigration entschlüsselt – IST Austria-Studie erscheint in Nature
Krebszellen und Leukozyten haben die Fähigkeit, sich relativ rasch einen Weg durch Körpergewebe zu bahnen. Wie es diesen mobilen Zellen gelingt, sich über große Distanzen hinweg fortzubewegen und weit entfernt von ihrem Entstehungsort zu überleben, ist noch nicht vollständig geklärt. Die Gruppe von Professor Michael Sixt am Institute of Science and Technology Austria (IST Austria) hat nun in einer im Fachmagazin Nature erscheinenden Studie einen Fortbewegungsmechanismus entschlüsselt, der es Zellen erlaubt, sich frei durch den Körper zu bewegen – insbesondere durch unwegsames Terrain.
Während sich die ganze Welt im Zuge der Corona-Krise im Lockdown befindet, begeben sich bestimmte Zellen in unserem Körper nach wie vor auf lange Reisen. Man muss auch keine Lungenentzündung entwickeln, der kleinste Schnitt in den Finger reicht bereits, um weiße Blutzellen – oder Leukozyten – dazu zu bewegen, umgehend die Blutgefäße zu verlassen und sich auf den Weg zur entzündeten Stelle zu machen. In ähnlicher Weise sind auch Krebszellen, die ihren Ursprung in jeglichem Gewebe oder Organ haben können, dazu in der Lage, sich im Körper auszubreiten und weit entfernt von ihrem Entstehungsort zu wachsen. Das Ergebnis: eine Metastase.
Üblicherweise bindet jede Zelle eines Organismus mittels spezifischer in der Plasmamembran sitzender Adhäsionsrezeptoren namens Integrine ans umliegende Gewebe. Als universelles „Bindemittel“ zwischen den Zellen und ihrer Umgebung halten die Integrine die Zelle entweder stabil an einem Ort oder dienen ihr als Verankerungen, während sie sich durchs Gewebe bewegen. Wie können jedoch bestimmte Zelltypen wie Leukozyten auf flexible Art und Weise durch verschiedene Gewebestrukturen krabbeln, obwohl diese Gewebe nicht unbedingt mit den notwendigen Molekülen ausgestattet sind, an die die Adhäsionsrezeptoren binden können?
Fortbewegung mit und ohne „Bindemittel“
Das Geheimnis wurde in der nun erschienenen Nature-Studie der Forschungsgruppe um Professor Michael Sixt am Institute of Science and Technology Austria (IST Austria) gemeinsam mit Kolleg_innen aus Frankreich gelüftet. Durch die Verschneidung praktischer Experimente mit physikalischen Modellen konnten die Wissenschafter_innen einen neuen Mechanismus der Zellfortbewegung beschreiben, der gänzlich unabhängig von spezifischen Bindungen an die extrazelluläre Umgebung funktioniert. Stattdessen machen sich die Zellen die Geometrie ihres unmittelbaren Umfeldes zunutze, um sich den für die Fortbewegung nötigen Vortrieb zu verschaffen.
Für ihre Experimente deaktivierten die Biolog_innen in verschiedenen Leukozyten die Funktion der Integrine mittels genetischer Methoden, um die Verbindung zwischen der Zelle und ihrer Umgebung zu trennen. Während Integrine unabdingbar für das Überleben und die Fortbewegung beinahe aller Zelltypen sind, konnten die IST Austria-Wissenschafter_innen bereits in einer früheren Studie demonstrieren, dass Leukozyten auch ohne Integrine auskommen. Dasselbe gilt für bestimmte Krebszellen.
Glatteis voraus!
Um die Mechanismen zu analysieren, die es den Zellen ermöglichen, sich ohne Adhäsion fortzubewegen, betrachteten die Wissenschafter_innen in den aktuellen Experimenten nicht die molekulare Zusammensetzung, sondern die Geometrie der Zellumgebung. Dazu bauten sie „Mikrofluidkanäle“ vom Durchmesser einer einzigen Zelle und mit unterschiedlicher Wandbeschaffenheit: von völlig glatt bis hin zu uneben und strukturiert. Indem die Wissenschafter_innen nun Leukozyten durch diese Kanäle schickten, konnten sie beobachten, dass sich die Integrin-befreiten Zellen in Kanälen mit glatten und parallelen Wänden nicht weiterbewegen konnten. „Die Zellen liefen sozusagen auf der Stelle wie die Reifen eines Autos, die auf eisigem Untergrund durchdrehen“, so Anne Reversat, Erstautorin der Studie, ehemalige Postdoc am IST Austria und nun als Forscherin an der University of Liverpool tätig. „Waren die Wände jedoch strukturiert oder uneben, hatten die Zellen keine Schwierigkeiten, auch ohne Integrine effizient voranzukommen. Zellen, die ihre Integrine nach wie vor einsetzen konnten, bewegten sich mühelos sowohl durch die strukturierten als auch durch die glatten Kanäle.“

Der richtige Grip für totale Bewegungsfreiheit
Bei näherer experimenteller wie theoretischer Betrachtung der Biomechanik dieser „Off-road“-Zellbewegungen, entdeckten Reversat et al. die mechanische Klammer beider Bewegungsformen: Aktin, die filamentöse Bausubstanz des Zytoskeletts der Zelle, fließt vom vorderen zum hinteren Zellende. Dieser „retrograde Aktinfluss“ erzeugt jene Kraft innerhalb der Zelle, die in unmittelbarer Folge der Koppelung an die Umgebung dem Zellkörper Vortrieb verleiht. Die Kraftübertragung kann dabei mittels Integrine passieren, die die Plasmamembran durchstoßen und dadurch das Aktin im Inneren der Zelle mit dem Substrat außerhalb der Zelle verbinden.
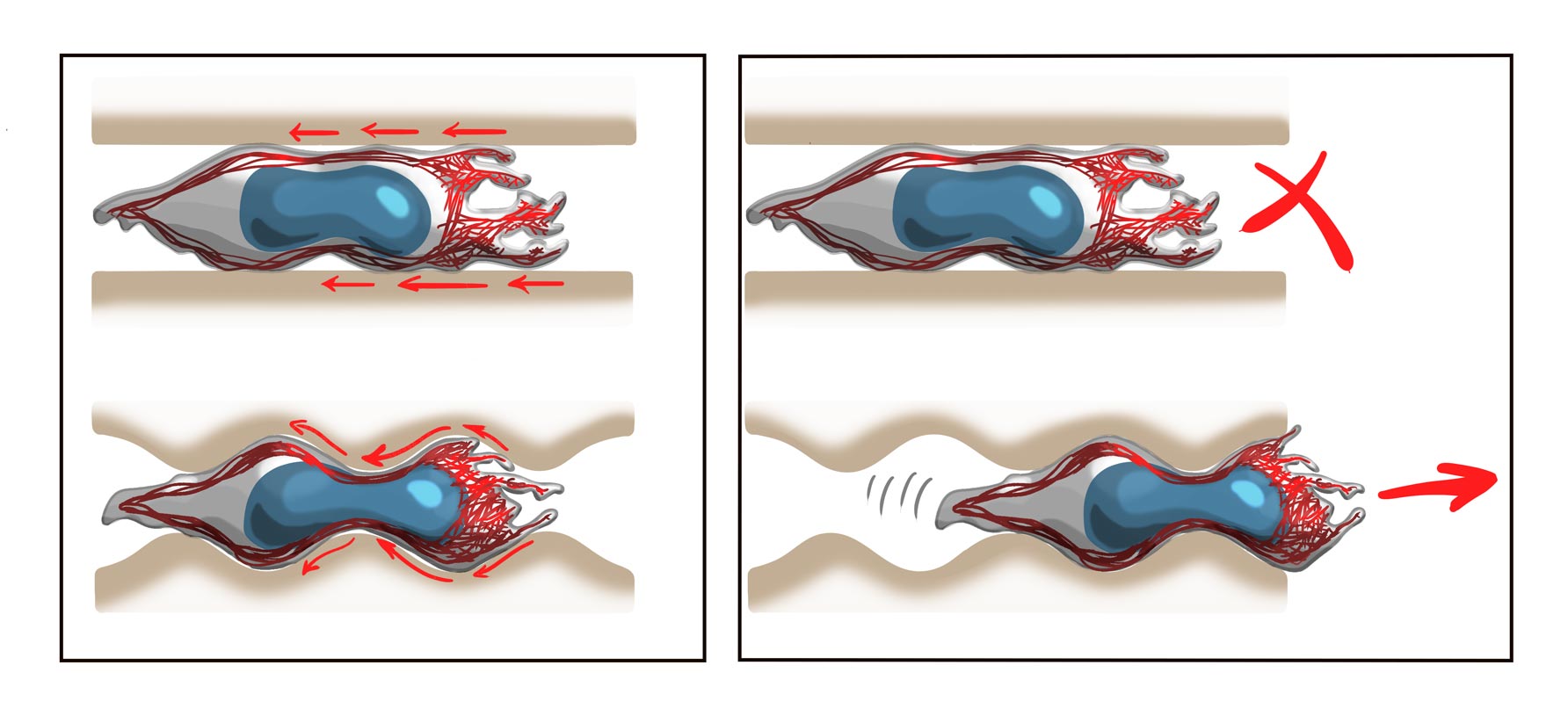
Wie die Wissenschafter_innen jedoch sowohl in ihren Experimenten als auch in einem theoretischen Modell zeigen konnten, kann Aktin die Verbindung mit der Umgebung nicht nur über die Integrine herstellen, sondern auch gänzlich unabhängig von jeglichen Transmembranrezeptoren. „Der retrograde Aktinfluss erzeugt im Inneren der Zelle Scherkräfte, die bei jeder Unebenheit Druck auf die Kanalwände ausüben. Sind die Wände glatt und parallel zueinander oder die Unebenheiten zu weit voneinander entfernt, funktioniert dieser Mechanismus nicht. Man könnte auch sagen, die Zelle hantelt sich vorwärts, indem sie ihre Form verändert“, erklärt Reversat. „Schließlich sind Leukozyten amöboide Zellen—vom griechischen Wort „amoibos“ für „wechselnd“. Nachdem die Feinstruktur von Geweben geometrisch komplex ist, können amöboide Zellen stets auf diese Art der Fortbewegung zurückgreifen. Dies macht sie unglaublich anpassungsfähig und sie können praktisch überall hingelangen.“
Zugehöriges Video auf YouTube ansehen
Ein Leukozyt bei der Migration durch einen Mikrofluidkanal ohne transmembrane Kraftübertragung. An Stellen, wo der Kanal zahlreiche Unebenheiten aufweist (links), kann sich die Zelle rasch fortbewegen. Sind die Unebenheiten jedoch zu weit auseinander oder ist die Kanalwand rundherum glatt, treten die Zellen auf der Stelle (rechts). © IST Austria – Sixt group
Publikation
Anne Reversat, Florian Gaertner, Jack Merrin, Julian Stopp, Saren Tasciyan, Juan Aguilera, Ingrid de Vries, Robert Hauschild, Miroslav Hons, Matthieu Piel, Andrew Callan-Jones, Raphael Voituriez & Michael Sixt. 2020. Adhesion-free cell migration by topography-1 based force transmission. Nature. DOI: 10.1038/s41586-020-2283-z
Förderinformation
Der am IST Austria durchgeführte Teil der Studie wurde finanziert vom Europäischen Forschungsrat (ERC Starting Grant Nr. 281556 und Consolidator Grant Nr. 724373) sowie durch Fördermittel des Wissenschaftsfonds FWF.



